Lektin Nedir?
Belirli bir karbonhidrata tersine çevrilebilir şekilde bağlanan en az bir katalitik olmayan alanın varlığı, bir proteinin lektin olarak adlandırılması için tek ön koşuldur. Sonuç olarak, bitki lektinleri, spesifik bir mono- veya oligosakkarite tersine çevrilebilir şekilde bağlanan en az bir katalitik olmayan alana sahip olan bitki proteinleri olarak tanımlanabilir.
Bir lektinin bir şeker kalıntısına bağlanması, antikorlar veya enzim substrat spesifikliği tarafından antijenik tanıma kadar spesifik olmasa da spesifiktir. Lektinler, karbonhidrat bağlanma özgüllüklerine göre farklı gruplara ayrılabilir, örneğin, mannoz bağlama, glikoz / mannoz bağlama, N-asetilglukozamin bağlama, galaktoz bağlama, N-asetilgalaktozamin bağlama, fukoz bağlama ve siyalik asit bağlama . Lektinler, çiçekli bitkiler, hayvanlar, mantarlar, sikadlar, eğrelti otları ve algler dahil olmak üzere çeşitli organizmalardan izole edilmiştir. Kan grubu özgüllüğü, antitümör, immünomodülatör, antifungal ve böcek önleyici (2) aktiviteler gibi çeşitli ilginç biyolojik aktiviteler sergilerler.
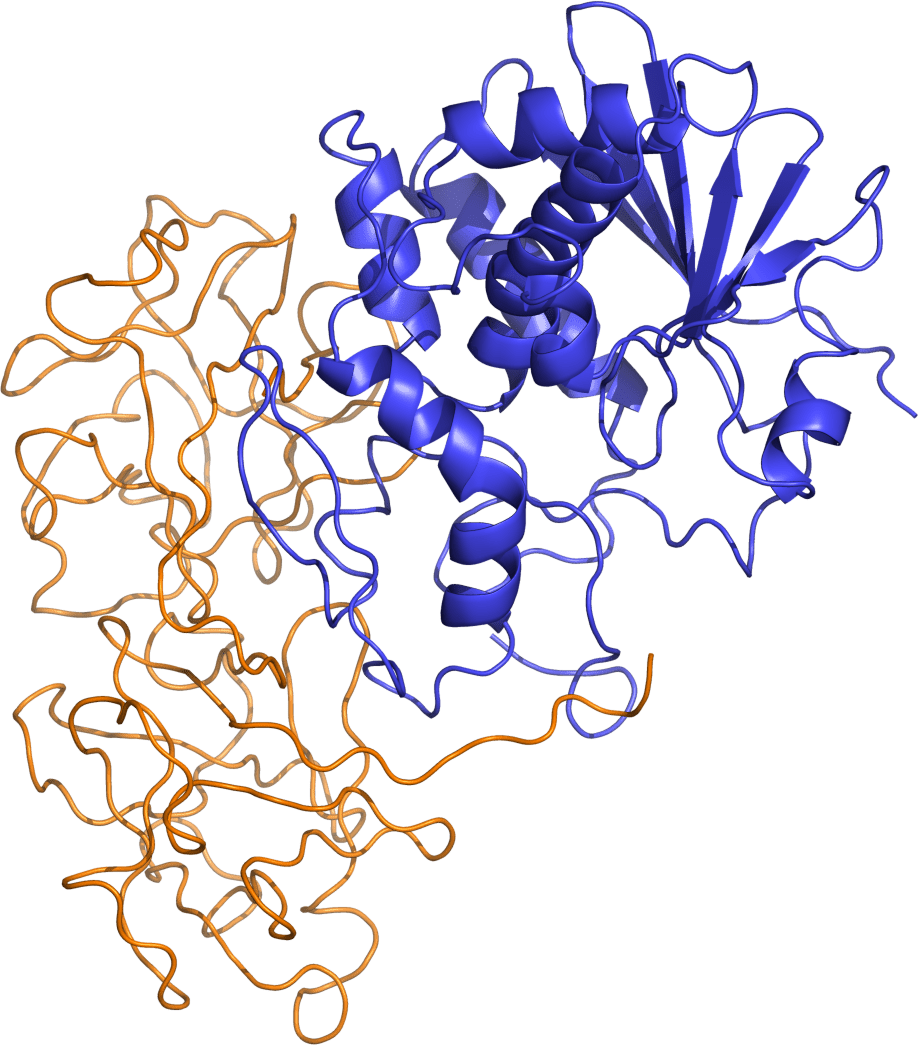
Pek çok bitki türü, genellikle lektin veya aglütinin olarak adlandırılan karbonhidrat bağlayıcı proteinler içerir. Genel olarak konuşursak, lektinler, spesifik mono- veya oligosakkaritlere tersine çevrilebilir şekilde bağlanan proteinlerdir. 1888’de Stillmark tarafından hint fasulyesi ekstraktlarında hemaglutinasyon faktörünün ilk keşfinden bu yana, bu proteinlerden birkaç yüz tanesi izole edildi. Karbonhidrat bağlanma özgüllükleri, moleküler yapıları ve biyokimyasal özellikleri açısından bazı ayrıntılarla karakterize edilmiştir. Farklı bitki türlerinden elde edilen lektinler, genellikle moleküler yapıları ve özgüllükleri açısından farklılık gösterir. Bu nedenle, bitki lektinlerinin yapay olarak yalnızca karbonhidratları tanıma ve bağlama yetenekleri temelinde birlikte sınıflandırıldığını anlamak önemlidir.
W J Peumans ve E J Van Damme‘ın “Lectins as plant defense proteins” makalesinden derlenmiştir.
Lektinlerin Fizyolojik Rolleri
Tamamen farklı bir yapıya ve şeker bağlama özgüllüğüne sahip proteinlerin aynı fizyolojik rolü yerine getirip getirmediği sorusuna cevap aranmaktadır. Çoğu bitki lektininin rolünün kesin olarak bilinmemesinin temel nedeni nedeniyle, bu soruya henüz kesin bir cevap verilemez. Bununla birlikte, çoğu lektinin bitkinin farklı bitki yiyen organizmalara karşı savunmasında rol oynadığına dair artan kanıtlar vardır. Lektinlerin bitki savunmasına dahil olabileceği fikri yeni değildir. Daha önceki bir incelemede, Chrispeels ve Raikhel (1991), fitohemaglutinin ailesinin ve bir dizi kitin bağlayıcı proteinin savunma rolünü eleştirel olarak değerlendirdiler.
Son birkaç yılda, genel olarak bitki lektinlerinin çalışılmasında ve özellikle diğer organizmalar üzerindeki etkilerinin anlaşılmasında önemli ilerleme kaydedilmiştir. Bu yazıda, bitki lektinlerinin savunma rolünü destekleyen bazı gelişmeler bulunmakta. Buna ek olarak, bu bitki proteinleri grubuna ilişkin mevcut bilgilerimiz ışığında bu alandaki önceki çalışmalara ait veriler ayrıca sunulmakta.
Lektin Tanımı, Lektin Proteini Özellikleri ve Terminoloji
Bitki savunmasındaki rollerini tartışmadan önce, lektin kavramının sınırları içinde kalan protein grubunu tanımlamalıyız. Lektin terimi başlangıçta bazı karbonhidrat bağlayıcı proteinlerin, belirli bir insan kan grubunun (Latince lejere fiilinden, “seçmek” anlamına gelir). Seçici olarak aglütine eritrositlerini aglütine etme kabiliyetine atıfta bulunmuştur. Lektin terimine sıkı sıkıya bağlı kalınmamıştır. Daha genel aglütinasyon davranışı gösteren a11 proteinlerine yaygın olarak uygulandığı için, “lektin” kelimesinin orijinal anlamı kayboldu. Bu açıdan bakıldığında, lektin ile eşanlamlı olarak kullanılan “aglutinin” daha doğrudur. Çünkü karbonhidrat bağlayıcı proteinlerin eritrositleri veya diğer hücreleri aglütine etme kabiliyetini ifade eder.
Lektinlerin, hücreleri aglütine eden karbonhidrat bağlayıcı proteinler, antikorlar, enzimler dışında karbonhidrat bağlayıcı proteinler olarak önceki tanımları, lektinlerin ve lektinle ilişkili proteinlerin tanımında güncelleme gerektirir.
Lektin Nedir? Fizyolojik Etkileri ve Sınıflandırılması
İlk olarak, bazı bitki enzimleri, bir karbonhidrat bağlayıcı ve bir katalitik alandan oluşan füzyon proteinleridir. Örneğin Sınıf I kitinazlar, bir “menteşe” bölgesi ile ayrılan bir kitin bağlayıcı alan ve bir katalitik alandan vardır (Collinge ve diğerleri, 1993). Benzer şekilde risin ve abrin de bu gruptadır. Tip 2 RIP‘ler, toksik bir A zincirinin ve bir karbonhidrat bağlayıcı B zincirinin (Barbieri ve diğerleri, 1993).
İkincisi, birkaç karbonhidrat bağlayıcı protein yalnızca bir bağlanma yerine sahiptir ve bu nedenle glikokonjugatları veya aglütine edici hücreleri çökeltemez. Örneğin, orkidelerden aglütinasyon yapmayan Man bağlayıcı proteinler, monomerler olarak oluşmaları haricinde aynı türden gelen dimerik Man’e özgü lektinlere çok benzerdir (Van Damme ve diğerleri, 1994). Üçüncüsü, birkaç baklagil türü, lektinlerle açıkça ilişkili olan ancak karbonhidrat bağlama aktivitesinden yoksun proteinler içerir. Bu protein grubunun iyi bilinen örnekleri, Pkaseolus vulgaris arcelinleri ve a-amilaz inhibitörüdür (Mirkov ve diğerleri, 1994).
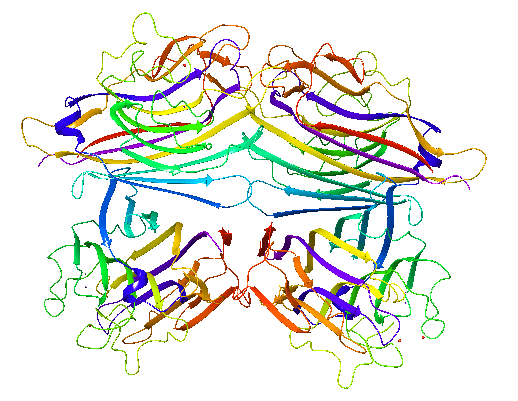
PDB: 2PEL
DOI: 10.2210/pdb2PEL/pdb
Belirli bir karbonhidrata tersine çevrilebilir şekilde bağlanan en az bir katalitik olmayan alanın varlığı, bir proteinin lektin olarak adlandırılması için tek ön koşuldur. Sonuç olarak, bitki lektinleri, spesifik bir mono- veya oligosakkarite tersine çevrilebilir şekilde bağlanan en az bir katalitik olmayan alana sahip olan bitki proteinleri olarak tanımlanabilir. Bu tanım, aglütinasyon ve / veya glikokonjugat çökelme özellikleri açısından oldukça farklı davranan geniş bir protein yelpazesini içerir.
Lektinlerin Sınıflandırılması
Genel yapılarına bağlı olarak üç ana tip lektin vardır. Bunlar: “merolektinler“, “hololektinler” ve “kimerolektinler” Merolektinler, yalnızca tek bir karbonhidrat bağlama alanından oluşmuş proteinlerdir. Küçük, tek polipeptit proteinleridir ve tek değerlikli yapıları nedeniyle glikokonjugatları veya aglütine edici hücreleri çökeltemezler. Bu grubun örnekleri, hevein (Van Parijs ve diğerleri, 1991) ve orkidelerden monomerik Man bağlayıcı proteinlerdir. Hololektinler ayrıca, yalnızca karbonhidrat bağlama alanlarından oluşturulur, ancak aynı veya çok homolog olan iki veya daha fazla bu tür alan içerir. Bu grup, çoklu bağlanma bölgelerine sahip olan ve dolayısıyla hücreleri aglütine edebilen veya glikokonjugatları çökeltebilen a11 lektinleri içerir.

PDB: 1Q9B
DOI: 10.2210/pdb1Q9B/pdb
Açıktır ki, bilinen bitki lektinlerinin çoğunluğu, hemagglutinin olarak davrandıkları için hololektinlerdir. Kimerolektinler, karbonhidrat bağlama alanından bağımsız olarak hareket eden, iyi tanımlanmış bir katalitik aktiviteye (veya başka bir biyolojik aktiviteye) sahip, ilişkisiz bir alan ile art arda dizilmiş bir karbonhidrat bağlama alanına sahip füzyon proteinleridir. Şeker bağlama yerlerinin sayısına bağlı olarak kimerolektinler, merolektin veya hololektin gibi davranır. Örneğin, B zincirlerinde (örn. Risin) iki karbonhidrat bağlanma bölgesi olan tip 2 RIP’ler, hücreleri aglütine ederken, tek bir kitin bağlama alanına sahip sınıf I bitki kitinazları yapmaz.
Lektin ve Fizyolojik Etkileri
Lektin, spesifik karbonhidrat bağlama aktiviteleriyle kendilerini diğer bitki proteinlerinden ayırır. Fizyolojik rollerinin şeker bağlama özelliklerini içerdiği makul bir şekilde varsayılabilir. Prensip olarak, herhangi bir lektin aracılı reaksiyon veya süreç içinde, lektinin bir glikokonjugat reseptörüne spesifik bağlanması ile ilgilidir. Bu reseptörün bitki içinde veya dışında yer almasından bağımsızdır). Bu nedenle, bitki lektinlerinin fizyolojik rolünün araştırılması her zaman doğal reseptörlerinin araştırılmasıyla yakından bağlantılıydı(ligand reseptör etkileşimi ile ilgili daha fazla bilgi için Tamoksifen Sitrat yazısını okuyunuz). Bu, farklı yapıdaki glikokonjugatların, ancak aynı (veya yapısal olarak benzer) karbonhidratlara sahip olduğu anlamına gelir, aynı lektin için reseptör görevi görebilir.
Bir bitki lektininin ilk keşfi, hint fasulyesi lektininin insan kırmızı kan hücrelerinin zarları üzerindeki glikokonjugatlara bağlanmasına dayanır. Bu konu ile daha çok bilgi için Risin Proteini yazısını okuyunuz.
Lektin reseptörlerinin bitkinin kendisinde bulunması gerektiği düşünülmekte. Bununla birlikte, endojen reseptörler (lektin bağlayıcılar olarak da adlandırılır) bulunmaya çalışılsa da çok iyi sonuçlar elde edilmemiştir. Böylece bu fikir yavaş yavaş terk edildi. Bazı enzimler(enzimler ile ilgili daha çok bilgi için Enzimler ve Genel Özellikleri yazısını okuyunuz) haricinde, örneğin bazı kitinazlar, glukanalar ve glikosidazlar, lektin sınıfındaki proteinler.
Mikroorganizmaların (yani bakteri ve mantarlar) yüzeyinde bulunan böcek veya memeli otçulların bağırsak yolu boyunca glikokonjugatları tanıyabilen ve bağlayabilen tek bitki proteinleri lektin sınıfındadır.
Mikrobiyal ve hayvansal glikanların çeşitliliği göz önüne alındığında, lektinlerin karbonhidrat bağlayıcı özelliklerinin geniş spektrumu, bitkinin farklı şeker içeren reseptörlere karşı tanıma molekülleri geliştirmesinin bir göstergesidir.
Bitkilerin Dış Etkenlere Karşı Kendini Savunması
Moleküler, biyokimyasal, hücresel, fizyolojik ve evrimsel argümanlar, lektinlerin bitki savunmasında rolü olduğunu göstermektedir. Bu rol için önemli bir argüman, bitki lektinlerinin diğer organizmaların glikokonjugatlarını bağladığının korunmasıdır. Birçok bitki lektini glikoz, mannoz veya galaktoz gibi basit şekerleri bağlayabilirler. Buna rağmen bitkilerde yaygın olmayan oligosakkaritlere çok daha yüksek bir afiniteye sahiptirler. Örneğin, kitin bağlayıcı bitki lektin proteinleri, mantarların hücre duvarının ve omurgasızların dış iskeletinin tipik bir bileşeni olan bir karbonhidratı tanır. Benzer şekilde, mürverden (Shibuya ve diğerleri, 1987) ve Muackiu amurensis’ten (Knibbs ve diğerleri, 1991) sialik asit bağlayıcı lektin proteinleri, bitkilerde bulunmaz. Ancak şekerin önemli bir karbonhidrat bileşeni olan bir şekere bağlanır. Aynı durum, tipik hayvan glikoproteinlerinin kompleks (değiştirilmiş) oligosakarit yan zincirlerine özel olarak bağlanan a11 lektinler için de geçerlidir.
Evrimsel Süreç ve Lektin Proteinin Savunma Mekanizmasında Yer Alması
Lektin proteinlerinin bitkinin yabancı organizmalar tarafından saldırıya en yatkın kısımlarıyla bulunması koruyucu üstlendiğine dair önemli bir argümandır. Tüm bitki sürekli bir zararlı ve hastalık tehdidine maruz kalsa da, bireyin veya türün hayatta kalmasında anahtar rol oynadıkları için bazı doku veya organların ekstra korumaya ihtiyacı vardır. Depo organları ve tohumları, potansiyel parazitler ve avcılar için en çekici bölgeler olduklarından ve aktif bir savunma sisteminden yoksun olabileceğinden (aktif olmayan metabolik durumları nedeniyle) özellikle savunmasızdır. Örneğin, tohum kaynaklı bir böceğin istila ettiği tohumlar veya bir tarla faresi tarafından tüketilen soğanlar artık yaşayamaz. Aksine, böcekler tarafından yarısı yenmesine rağmen büyüyen bir bitki hayatta kalabilir ve hatta canlı yavrular üretebilir.
Bitkilerin evrimsel adaptasyonu hesaba katıldığında, depolama organlarını ve tohumlarını korumak için (pasif) savunma sistemleri geliştirdikleri makul bir şekilde iddia edilebilir. Bu bakış açısından, tipik depolama organlarında görülen lektin birikimi kesinlikle gösterge niteliğindedir. Dahası, bu lektin proteinlerinin çoğu büyük miktarlarda bulunduğundan ve ek olarak depolama proteinleri olarak davrandığından, bazı bitkiler nitrojen rezervlerinin bir kısmını karbonhidrat bağlayıcı proteinler olarak biriktirirler.
Lektin Protienlerinin Savunmada Rol Oynadğına Dair Kesin Delil
Tip 2 RIP’lerin güçlü sitotoksik ajanlar olduğu bilinmektedir. Şeker bağlayıcı B zinciri, hücre yüzeyindeki bir (glikokonjugat) reseptörüne bağlanarak A zincirinin alımını teşvik eder. Hücreye girdikten sonra, A zinciri, büyük rRNA’nın tek bir adenosin kalıntısının N-glikosidik bağını ayırarak ökaryotik ribozomları katalitik olarak etkisiz hale getirir. Prensip olarak, tip 2 RIP’ler, sitoplazmaya ulaşırlarsa, a11 ökaryotlar için son derece toksiktir. Bu konuyu risin proteini yazısında ayrıntısıyla tartışmıştık.
Tip 2 RIP’lerin hayvanlar (insanlar dahil) üzerindeki ölümcül etkisi eski zamanlardan beri bilinmektedir. Böcekler, tip 2 RIP’ler ile temas ettiklerinde ise farklı tepki veriyor gibi görünüyorlar. Ricin, koleoptera Callosobruchus maculatus ve Anthonomus grandis için oldukça toksikti, ancak lepidoptera Spodoptera litoralis ve Heliothis virescens üzerinde hiçbir etkiye sahip değildi (Gatehouse ve diğerleri, 1990).
Bazı böceklerin risin içeren bir diyette hayatta kalması, onların ya toksini etkisiz hale getirebileceklerini ya da toksini bağlamadıklarını gösterir. Diğer bir tip 2 RIP, yani kış akonitinden elde edilen lektin (Eranthis hyemalis) (Kumar ve diğerleri, 1993), Diabrotica undecimpunctata (mısırın başlıca böcek zararlısı) larvaları için çok toksikti. Bu nedenle, tip 2 RIP’lerin bitkiye hayvanlara ve muhtemelen bazı böceklere karşı iyi koruma sağlaması muhtemel görünüyor.
Prensip olarak, tip 2 RIP’ler ayrıca mantarlar için toksiktir. Bununla birlikte, sitoplazmaya nüfuz edemedikleri için, istilacı mantarlar üzerinde doğrudan zararlı bir etkiye sahip olduklarını düşünmek zordur. Bakteriyel ribozomlar(ilaç keşfi ile ilgili daha çok bilgi için Docking ve Kanser Tedavisinde Kullanımı adlı yazıyı okuyunuz), tip 2 RIP’lere karşı duyarsızdır. Bu da bu toksinlerin bakteriler üzerinde herhangi bir doğrudan etki yapamayacağı anlamına gelir. Şaşırtıcı bir şekilde, tip 2 RIP’ler, etki mekanizması bilinmemekle birlikte, bitki virüslerine karşı inhibe edici bir aktivite sergiler. Muhtemelen enfektivite testleri için kullanılan virüs süspansiyonunda bulunan RIP’ler ribozomları etkisiz hale getirmektedir. Ve yaralı bitki hücrelerini öldürerek bir tür aşırı duyarlı tepkiye neden olmaktadırlar.
Bitki Lektinlerinin Antiviral Etkileri
Yukarıda açıklanan lektin tip 2 RIP’ler haricinde, başka hiçbir bitki lektininin viral enfeksiyonu, replikasyonu veya sistemik yayılmayı inhibe ettiği bildirilmemiştir. Bu kanıt eksikliği, bitki lektinlerinin olası bir antiviral etkisinin olmadığını göstermemektedir. Bitki virüsleri üzerinde glikanların yokluğu göz önüne alındığında bu durum mantıklı görünmektedir. Bu bağlamda, bitki lektin proteinlerinin, viryonlarında glikoproteinlere sahip olan hayvan ve insan virüsleri için in vitro olarak güçlü inhibitörleri olduklarından bahsetmeye değer kanıtlar vardır. (Balzarini ve diğerleri, 1992). Bazı bitki lektinlerinin dolaylı bir antiviral rolü olabileceği anlamına gelir. Örneğin böcek öldürücü lektinlerin varlığı, böceklerle bulaşan viral hastalıkların yayılmasını önleyebilir ve / veya azaltabilir. Antiviral ajanların tasarlanması, geliştirilmesi ve üretimi ile ilgili daha fazla bilgi için Favicovir Kullananlar için Ayrıntılı İnceleme ve Koronavirüs İlaç Geliştirme Çalışmaları adlı yazıları okuyunuz.
Bitki Lektinlerinin Antibakteriyal Etkisi
Bakterilerin hücre duvarı, yalnızca zarları üzerindeki glikokonjugatlar ile karbonhidrat bağlayıcı proteinler arasındaki herhangi bir etkileşimi engellemekle kalmaz, aynı zamanda bu proteinlerin sitoplazmaya nüfuz etmesini de önler. Bu nedenle bitki lektin proteinleri, zarın yapısını ve / veya geçirgenliğini değiştiremez veya istilacı mikropların normal hücre içi süreçlerini bozamaz.
Lektin proteinleri bitkinin bakterilere karşı savunmasında rol oynuyorsa, bunun hücre duvarı karbonhidratları veya hücre dışı glikanlar ile etkileşimlere dayanan dolaylı bir mekanizma yoluyla olması gerekir. Örneğin, (bir hücre duvarı proteini olarak kabul edilen) patates lektininin hücre duvarında Pseudomonas solanacearum’un avirülan suşlarını hareketsizleştirdiği öne sürülmüştür (Sequeira ve Graham, 1977). Virülan suşlar, lektin tarafından tanınmadı, hücre duvarına bağlanmadan kurtuldu ve bu nedenle çoğalarak bitkiye yayılabildiler. Ne yazık ki, patates lektininin varsayılan antibakteriyel aktivitesi, bilinmeyen saflıkta lektin preparatları ile yapılan in vitro deneylerden çıkarılmıştır.
Bitki Lektin Protienlerinin Antibakteriyal Etkisi için Litaratür Bulguları
Diğer bir dolaylı savunma mekanizması, dikenli elma (Datura stramonium) tohum lektini tarafından hava-su arayüzünde normal hareketli bakterilerin hareketlerinin engellenmesidir (Broekaert ve Peumans, 1986). Bu deneylerde esasen saf lektin preparatları kullanıldığından ve etkiler fetuin tarafından tamamen tersine çevrilmiştir. Bu hareketlilik kaybının lektine neredeyse kesin olarak atfedilmesini sağlamıştır. İn vitro bakteri hareketliliği, lektinin tohum kabuğundan ve tohum epiderminden hızlı ve yüksek oranda spesifik salınımı (emilim sırasında) ile ilişkilendirilmiştir. Lektin, toprak bakterilerinin çimlenen tohuma doğru kemotaktik hareketine karşı koyarak, fide köklerinin potansiyel olarak zararlı bakteriler tarafından istilasını önleyebilir.
Bitki Lektinlerinin Antibakteriyal Etkilerine Dair Kesin Bulgu Yoktur
Bitki lektinlerinin bakteri hücre duvarı peptidoglikanlarına bağlanmasıyla ilgili son araştırmalar iyi incelenmelidir. Birkaç baklagil tohumu lektininin muramik asit, N-asetilmuramik asit ve muramil dipeptid ile güçlü bir şekilde etkileşime girdiğini gösterilmiştir. Lektin proteinleri bitkinin mikroplara karşı savunmasındaki rolü hafife alınmış olabilir ( Ayouba ve diğerleri, 1994).
Enzim aktivitesi ve buna bağlı inhibisyon mekanizmalarını anlamak için genel bilgilerin irdelendiği Glutatyon Redüktaz Enzim Aktivitesi ve Enzim İnhibitörü ve İnhibisyon Çeşitleri adlı yazıları okuyunuz.
Bitki Lektinlerinin Mantarlar Üzerindeki Etkisi
Bitki lektinleri, kalın ve sert bir hücre duvarı varlığından dolayı mantar zarları üzerindeki glikokonjugatlara bağlanamaz. Hücrelerin sitoplazmasına nüfuz edemez. Bu organizmaların büyümesine ve gelişmesine doğrudan bir müdahale olası görünmemektedir. Bununla birlikte, lektinlerin mantar hücre duvarının yüzeyinde açığa çıkan karbonhidratlara bağlanmasına dayanan dolaylı etkiler mümkündür.(Purification and characterization of a lectin from endophytic fungus Fusarium solani having complex sugar specificity)
Isırgan otu lektininin kesin mekanizması henüz aydınlatılmamıştır, ancak kesinlikle bir kitinaz aktivitesine dayanmamaktadır ve mantar hücrelerinin normal metabolizmasını etkilememektedir. Bozulmuş kitin sentezi ve / veya birikiminin bir sonucu olarak sadece hücre duvarının sentezinin etkilendiği görülmektedir (Van Parijs ve diğerleri, 1992). Isırgan otu lektin proteinin in vitro antifungal aktivitesine rağmen, in vivo herhangi bir koruyucu aktiviteye sahip olup olmadığı hala bilinmemektedir. Çünkü lektin, filizlenen sporları veya miselyumu öldüremez. Isırgan otu lektininin mantar hücre duvarı üzerindeki değiştirici etkileri ve hif yapısının morfolojisi göz önüne alındığında, ısırgan lektin proteinin rizomların endomikorhiza tarafından kolonizasyonunun kontrolünde rol oynadığına inanılmıştır. Böyle bir rol, lektinin rizomlardaki ve tohumlardaki konumu ile kısmen uyum içindedir.
Daha fazla bilgi için tıklayın.
Lektin Proteinlerinin Zararlı Böcekler Üzerindeki Etkisi
Fitofajlı böceklerin sindirim sistemi boyunca yer alan epitel hücreleri, doğrudan diyet içeriğine maruz kalır ve bu nedenle, bitki savunma proteinleri için olası hedef bölgelerdir. Glikoproteinler bu zarların ana bileşenleri olduğundan, bağırsağın lümen tarafı tam anlamıyla diyet lektinleri için potansiyel bağlanma bölgeleri ile kaplıdır. Bir lektin protein bir glikoprotein reseptörüne bağlanması, lokal veya sistemik bir zararlı etki yarattığından, zararlı böcek türlerinin engelleneceğini düşünebiliriz.
PHA, bruchid böceği Callosobruckus maculatus’un (c’owpea biti) larvaları üzerindeki zararlı etkisine dayanarak böcek önleyici özelliklerin atfedildiği ilk lektindir. İronik bir şekilde, lektinlerin böceklere karşı koruyucu bir rolünün bu ilk göstergesi, etkilerin kontamine edici bir a-amilaz inhibitöründen kaynaklanması nedeniyle yanlış pozitif bir sonuca dayanıyordu (Huesing ve diğerleri, 1991b).
Daha yeni deneyler, buğday tohumu, patates yumruları ve yer fıstığı, dikenli elma (Dntura strmonium) ve osage portakalından (Maclura pomifera) elde edilen lektinlerin, kurde biti larvalarının gelişimi üzerinde önleyici bir etkiye sahip olduğunu gösterdi. Bununla birlikte, fizyolojik bir konsantrasyonda sadece WGA aktifti (Murdock ve diğerleri, 1990). Pirinçten (Oryza sativa) ve ısırgan otundan kitin bağlayıcı lektinler de börülce böceğinin larva büyümesini inhibe etti (Huesing ve diğerleri, 1991a). Ancak bu tipik tohum avcısının, niost bitki lektinlerine karşı duyarsız olduğu ve sadece orta derecede etkilendiği görülmektedir.
Yüksek Yapılı Canlılar ve Lektin Zehirlenmesi
Böceklerde olduğu gibi, yüksek hayvanların sindirim sistemi boyunca epitel hücreleri tamamen diyet içeriğine maruz kalır. Bu nedenle, bitkilerin bu bölgede bir etkileşim yoluyla hareket eden avcılara karşı savunma proteinleri geliştirmesi beklenebilir. Sindirim sisteminin lümen bölgesindeki hücreler, membran glikoproteinleri ve yüksek oranda glikosile edilmiş müsinlerle kaplı olduğundan, diyet bitki lektinleri ile etkileşim için sayısız hedef vardır.
Lektinlerin çeşitliliği ve hayvansal glikanlar için özgüllükleri göz önüne alındığında, bu proteinlerin bitkileri hayvan avcılarına karşı koruduğu tahmin edilebilir. Neyse ki, gıda ve yem üretiminde kullanılan bitkilerde bulunan lektinlerin olası sağlık riskini değerlendiren çalışmalar nedeniyle lektinlerin toksisitesi iyi belgelenmiştir. Bitki lektinlerinin toksik özellikleri hayvanlarda ve insanlarda tetikledikleri etkiler hakkındaki mevcut bilgilerimizin büyük bir kısmı, saflaştırılmış PHA ile besleme deneylerinden ve çiğ veya yetersiz pişirilmiş fasulye tarafından insanların kazara zehirlenmesinden elde edilmiştir. Bağırsak proteazlarına oldukça dirençli olan sindirilen PHA, hızla endositozlandığı bağırsağın fırça kenar hücrelerine bağlanır. Lektin hücrelere girdiğinde, sonunda ince bağırsağın hiperplazisine ve hipertrofisine yol açan gelişmiş bir metabolik aktiviteye neden olur (Pusztai ve diğerleri, 1990). Dahası, PHA veya çiğ fasulyenin yutulması akut mide bulantısına ve ardından kusmaya ve ishale neden olur. PHA’nın şiddetli etkileri, yırtıcı hayvanlara karşı korunmada lektinlerin potansiyelini göstermektedir.
Toksik lektinlerle ilgili araştırmaların çoğu PHA ile yapılmış olsa da, diğer lektinlerin benzer etkileri tetiklediğine dair birçok kanıt vardır. Örneğin, siyah çekirge (Robinia pseudoacacia) ve mürver (Sambucus nigra) kabuğunun lektinleri PHA ile aynı şiddetli toksisite semptomlarına neden olur. Her iki kabuk lektin proteini de bol olduğu için, mürver ve kara çekirge asla kemirgenler, geyikler veya diğer yaban hayatı tarafından saldırıya uğramazlar. Ancak çevredeki lektinsiz türlerin, ör. kavak, söğüt ve yabani elma, aynı hayvanlar için en sevilen besindir
Sonuç
Çoğu bitki lektin proteini, bitkinin savunmasında rol oynar. Virüslere ve mikroorganizmalara doğrudan müdahale oldukça istisnai iken, bitki lektin proteinlerinin yırtıcı omurgasızlar ve daha yüksek yapılı canlılar üzerindeki zararlı etkileri açıktır. Depolama organlarındaki lektin proteinlerinin bolluğu göz önüne alındığında, bitkilerin nitrojen rezervlerinin bir kısmını, pasif savunma proteinleri olarak kullanılabilen karbonhidrat bağlayıcı proteinler şeklinde biriktirdiğine inanmak için güçlü deliller vardır. Yeni yazılardan Antimalaryal İlaçlar – Yapı Bazlı İlaç Tasarımı ve Favipiravir Nedir? Favipiravir Yan Etkileri Nelerdir? adlı yazılar protein yapılar hakkında daha fazla bilgi vermektedir.
Lektin ile İlgili Bİlgilerin Elde Edildiği Kaynaklar Dizisi
Kaynaklar 1
- Barbieri L, Battelli MG, Stirpe F. Ribosome-inactivating proteins from plants. Biochim Biophys Acta. 1993 Dec 21;1154(3-4):237–282. [PubMed] [Google Scholar]
- Broekaert WF, Mariën W, Terras FR, De Bolle MF, Proost P, Van Damme J, Dillen L, Claeys M, Rees SB, Vanderleyden J, et al. Antimicrobial peptides from Amaranthus caudatus seeds with sequence homology to the cysteine/glycine-rich domain of chitin-binding proteins. Biochemistry. 1992 May 5;31(17):4308–4314. [PubMed] [Google Scholar]
- Broekaert WF, VAN Parijs J, Leyns F, Joos H, Peumans WJ. A chitin-binding lectin from stinging nettle rhizomes with antifungal properties. Science. 1989 Sep 8;245(4922):1100–1102. [PubMed] [Google Scholar]
- Chrispeels MJ, Raikhel NV. Lectins, lectin genes, and their role in plant defense. Plant Cell. 1991 Jan;3(1):1–9. [PMC free article] [PubMed] [Google Scholar]
- Collinge DB, Kragh KM, Mikkelsen JD, Nielsen KK, Rasmussen U, Vad K. Plant chitinases. Plant J. 1993 Jan;3(1):31–40. [PubMed] [Google Scholar]
Kaynaklar 2
- Kumar MA, Timm DE, Neet KE, Owen WG, Peumans WJ, Rao AG. Characterization of the lectin from the bulbs of Eranthis hyemalis (winter aconite) as an inhibitor of protein synthesis. J Biol Chem. 1993 Nov 25;268(33):25176–25183. [PubMed] [Google Scholar]
- Mirkov TE, Wahlstrom JM, Hagiwara K, Finardi-Filho F, Kjemtrup S, Chrispeels MJ. Evolutionary relationships among proteins in the phytohemagglutinin-arcelin-alpha-amylase inhibitor family of the common bean and its relatives. Plant Mol Biol. 1994 Nov;26(4):1103–1113. [PubMed] [Google Scholar]
- Pusztai A, Ewen SW, Grant G, Brown DS, Stewart JC, Peumans WJ, Van Damme EJ, Bardocz S. Antinutritive effects of wheat-germ agglutinin and other N-acetylglucosamine-specific lectins. Br J Nutr. 1993 Jul;70(1):313–321. [PubMed] [Google Scholar]
- Pusztai A, Ewen SW, Grant G, Peumans WJ, van Damme EJ, Rubio L, Bardocz S. Relationship between survival and binding of plant lectins during small intestinal passage and their effectiveness as growth factors. Digestion. 1990;46 (Suppl 2):308–316. [PubMed] [Google Scholar]
- Shibuya N, Goldstein IJ, Broekaert WF, Nsimba-Lubaki M, Peeters B, Peumans WJ. The elderberry (Sambucus nigra L.) bark lectin recognizes the Neu5Ac(alpha 2-6)Gal/GalNAc sequence. J Biol Chem. 1987 Feb 5;262(4):1596–1601. [PubMed] [Google Scholar]
- Van Damme EJ, Balzarini J, Smeets K, Van Leuven F, Peumans WJ. The monomeric and dimeric mannose-binding proteins from the Orchidaceae species Listera ovata and Epipactis helleborine: sequence homologies and differences in biological activities. Glycoconj J. 1994 Aug;11(4):321–332. [PubMed] [Google Scholar]